- La valencia determina la proporción de los distintos iones intervinientes, para asegurar la electroneutralidad.
- Además, los iones eligen la configuración más estable (disposición de aniones y cationes que maximiza la atracción y minimiza la repulsión electrostática). Mayor estabilidad mientras mayor sea el número de coordinación. Para alcanzar la mayor estabilidad, debe existir «contacto real» entre los iones de distinto signo (la gran proximidad de iones del mismo signo genera fuerte repulsión).
 |
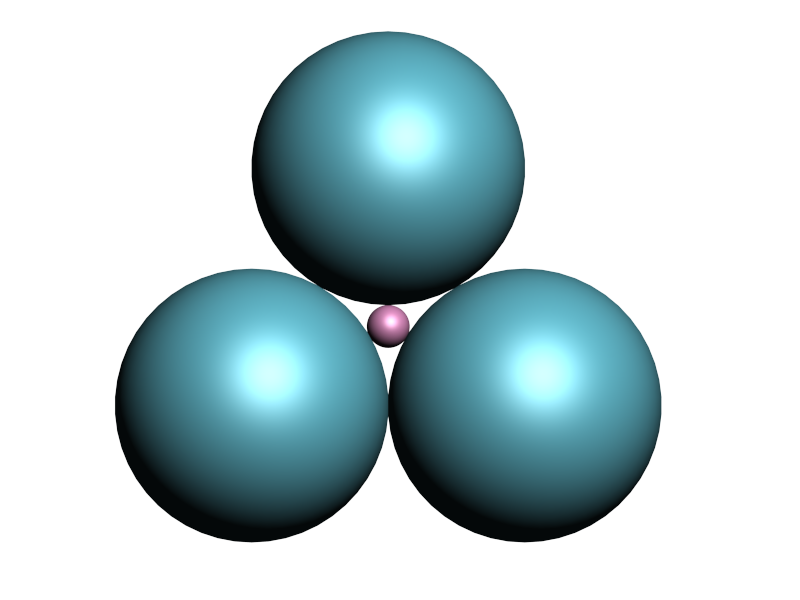 |
 |
| Estable | Estable crítica | Inestable |
La relación de radios iónicos determinará la configuración más estable.
| Relación de radios | Número de coordinación | Tipo de coordinación | Poliedro de coordinación |
| \(x=\frac{r_{\texttt{A}}}{r_{\texttt{B}}}\) | (Z) | ||
| \(0< x< 0.155\) | 2 | Lineal |  |
| \(0.155\leq x< 0.225\) | 3 | Triangular |  |
| \(0.225\leq x< 0.414\) | 4 | Tetraédrica |  |
| \(0.414\leq x< 0.732\) | 6 | Octaédrica | 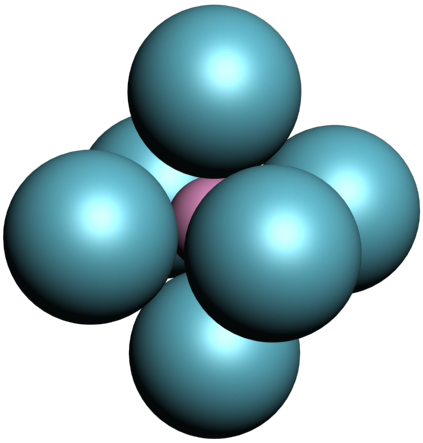 |
| \(0.732\leq x< 1\) | 8 | Cúbica |  |
| \( x= 1\) | 12 | Cuboctaédrica |  |